2024年6月22日,一篇題為"Robust anti-tumor immunity through the integration of targeted lipid nanoparticle-based mRNA nanovaccines with PD-1/PD-L1 blockade "的研究論文,發表在《Materials Today Bio》雜志上。

本研究創新構建了一種靶向納米疫苗平臺,利用艾特森MPE-L2型微流控制備儀制備甘露糖修飾的脂質納米顆粒(TLNP),同時負載腫瘤抗原mRNA(如mOVA)和cGAMP(環磷酸鳥苷-腺苷酸)佐劑,形成靶向納米疫苗(TNVs),實現對抗原呈遞細胞的特異性靶向,提升抗原遞送與免疫激活效率。通過優化mRNA疫苗的靶向遞送能力,并與免疫檢查點阻斷療法結合,解決傳統mRNA疫苗遞送不足、免疫激活有限及腫瘤微環境抑制的問題,最終增強抗腫瘤免疫應答。

作用機制
靶向納米疫苗(TNVs)進入抗原呈遞細胞(APCs)后,其攜帶的mRNA翻譯生成腫瘤抗原,經MHCⅠ/Ⅱ類分子呈遞,激活CD8?細胞毒性T細胞與CD4?輔助T細胞,而抗PD-L1抗體通過阻斷腫瘤細胞PD-L1與T細胞PD-1的結合逆轉免疫抑制,二者協同作用可增強腫瘤浸潤免疫細胞活性,誘導免疫記憶,從而抑制腫瘤復發與轉移。

圖例1:靶向納米疫苗制備與作用機制
? 配方摩爾比:
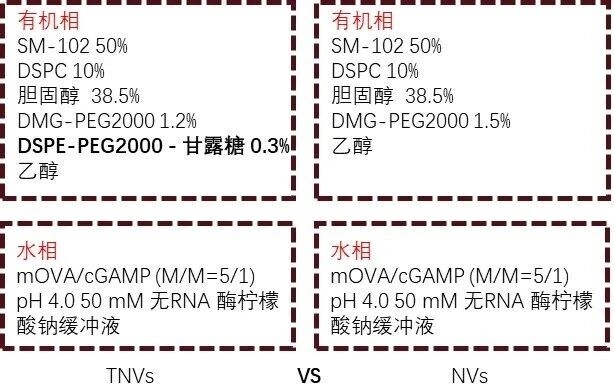
圖例2:靶向納米疫苗配方摩爾比
1. 納米疫苗的設計與表征
首先,研究團隊通過微流控技術制備了非靶向(NVs)與靶向(TNVs)兩種納米疫苗,并完成表征與穩定性驗證,結果顯示二者粒徑均為80-85nm、PDI:0.05-0.09,呈均一球形,mRNA包封率超97%,且4℃儲存在28天內性能穩定,為后續實驗提供了合格的載體基礎。
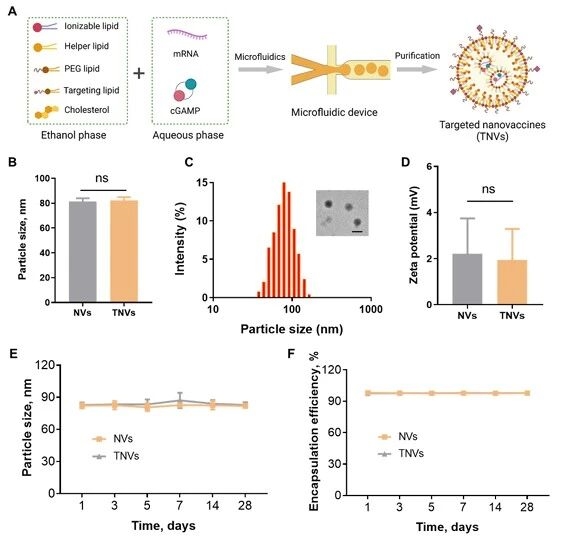
圖例3:納米疫苗的制備與表征
2. 納米疫苗在 BMDCs中的生物學功能
接著,在骨髓來源樹突狀細胞(BMDCs)中探究納米疫苗的生物學功能,發現兩種疫苗均具有良好生物相容性,而TNVs憑借甘露糖受體介導的靶向作用,實現高效內吞,其mRNA轉染效率顯著高于NVs,接近陽性對照水平,明確了靶向設計的優勢。

圖例4:納米疫苗在BMDCs中的生物學功能
3. 納米疫苗對BMDCs的免疫調節作用
其次,進一步分析納米疫苗對BMDCs的免疫調節作用,結果表明TNVs能更有效地促進APC成熟、增強抗原交叉呈遞能力,同時通過cGAMP激活STING-IRF3通路,顯著上調IL-12p70、TNF-α等細胞因子分泌,驗證了疫苗在體外的免疫激活潛力。
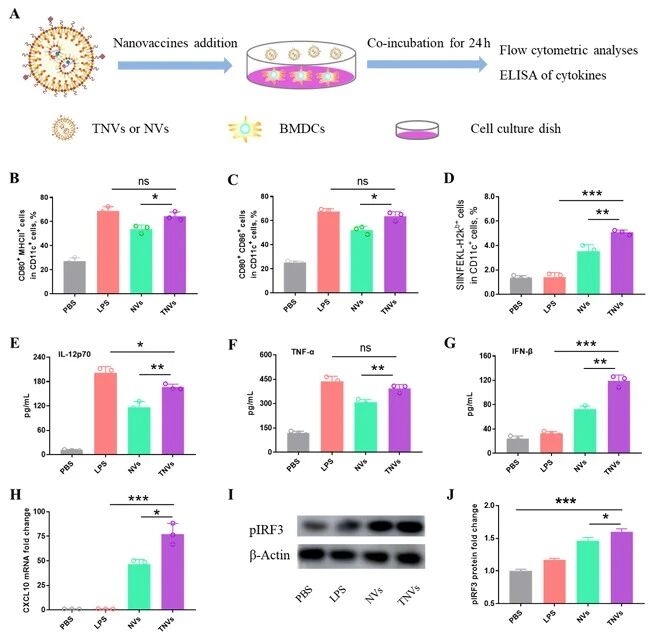
圖例5:納米疫苗對BMDCs的免疫調節作用
4.納米疫苗在體內的免疫調節效果
隨后,在體內環境中驗證納米疫苗的免疫調節效果,體內轉染實驗顯示TNVs局部表達效率更高,經三次肌肉注射免疫后,小鼠腹股溝淋巴結中成熟DC比例、抗原交叉呈遞效率及血清促炎細胞因子水平均顯著提升,證實靶向疫苗在體內仍能高效激活免疫應答。
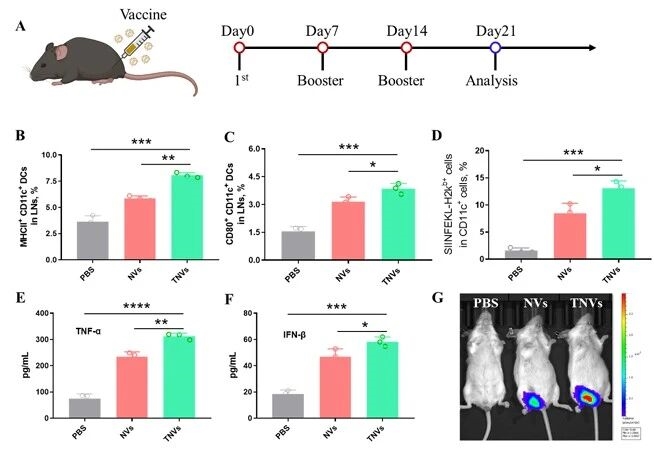
圖例6:納米疫苗在體內的免疫調節效果
5. 治療性納米疫苗的抗腫瘤效果
在此基礎上,評估治療性納米疫苗的抗腫瘤效果,在LLC-OVA荷瘤小鼠模型中,TNVs治療組腫瘤體積顯著縮小,腫瘤組織中抗腫瘤免疫細胞浸潤增加,但同時觀察到腫瘤細胞PD-L1表達上調,這為后續聯合PD-L1阻斷療法提供了關鍵實驗依據。
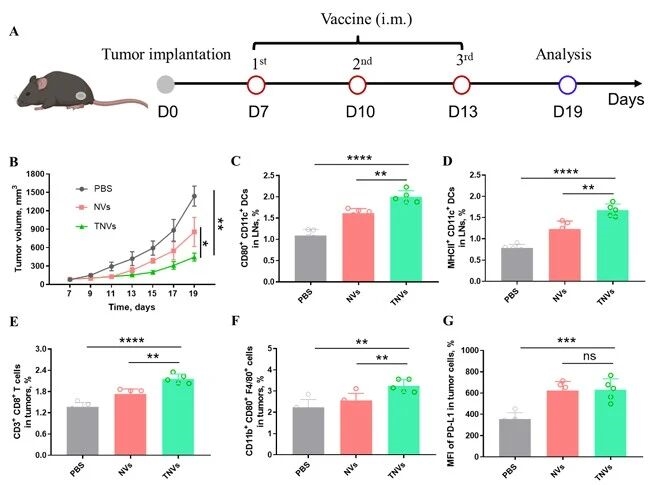
圖例7:治療性納米疫苗的抗腫瘤效果
6. TNVs聯合抗PD-L1抗體的協同治療效果
進而,考察TNVs與抗PD-L1抗體的協同治療效果,發現聯合治療組腫瘤抑制效果優于單藥治療,腫瘤壞死區域擴大,且在預防性免疫模型中能延長小鼠生存期,腫瘤再挑戰實驗證實其可誘導免疫記憶、抑制復發,凸顯了聯合策略的優勢。

圖例8:TNVs聯合抗PD-L1抗體的協同治療效果
7. 聯合治療的抗腫瘤機制解析
為明確聯合治療的作用機制,進一步分析發現,聯合組不僅能提升淋巴結中成熟DC比例,還能重塑腫瘤微環境,增加抗腫瘤免疫細胞浸潤、減少免疫抑制細胞比例,同時上調血清促炎細胞因子水平,免疫熒光結果也驗證了這一免疫調節趨勢。
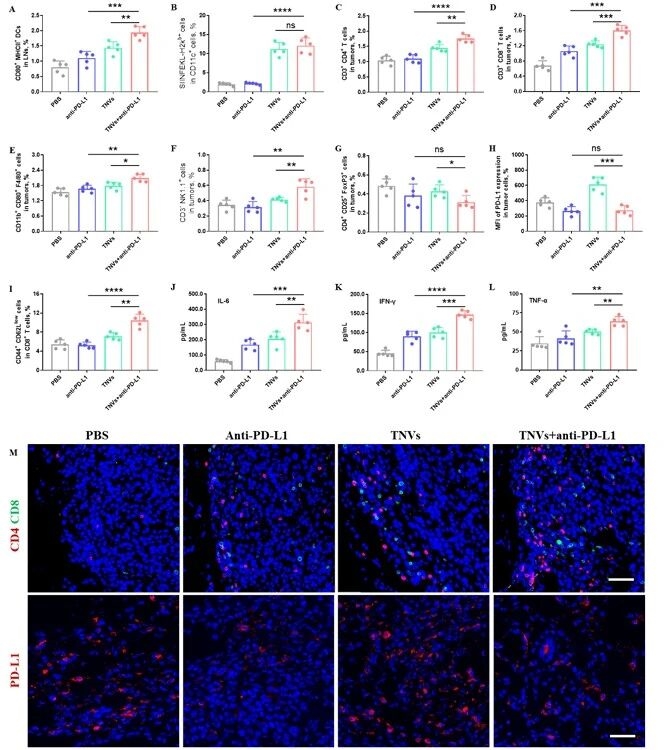
圖例9:聯合治療的抗腫瘤機制解析
8. 生物安全性評估
最后,開展生物安全性評估,各治療組小鼠的血常規、肝腎功能指標均無顯著異常,主要器官未出現明顯病理損傷,長期毒性實驗也未發現安全隱患,最終證實該聯合治療策略兼具強效抗腫瘤效果與良好的生物安全性。
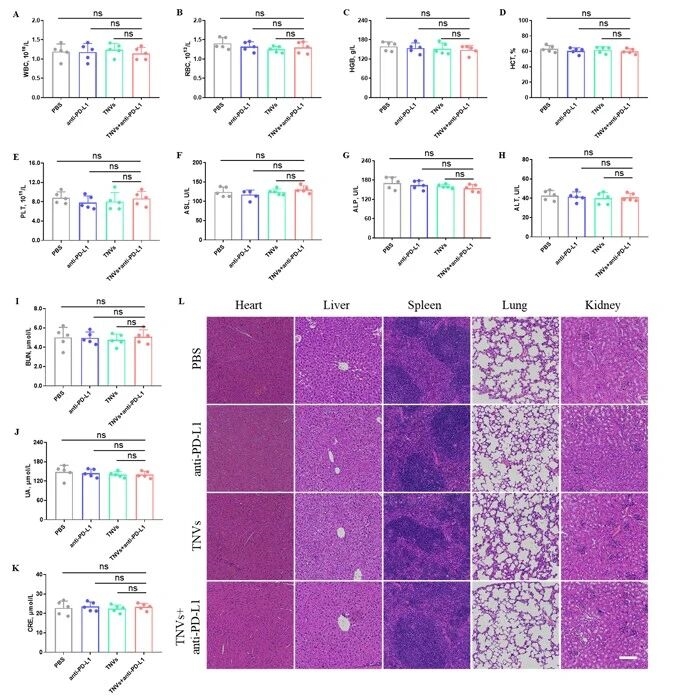
圖例10:生物安全性評估
知識分享:研究亮點
1 精準靶向遞送系統:通過甘露糖修飾脂質納米顆粒,結合微流控技術,實現對抗原呈遞細胞的特異性靶向,提升mRNA和佐劑的遞送效率與免疫激活效果;
2 協同抗腫瘤策略:將靶向納米疫苗與抗PD-L1抗體聯合,前者激活免疫應答,后者解除腫瘤免疫抑制,形成協同效應,增強抗腫瘤效果并誘導免疫記憶;
3 多功能納米平臺設計:同步負載mRNA抗原與cGAMP佐劑,兼具抗原遞送和免疫刺激功能。
Materials Today Bio (IF 10.2) Pub Date:2024-06-22,DOI: 10.1016/j.mtbio.2024.101136.












立即詢價
您提交后,專屬客服將第一時間為您服務