研究背景
生命的延續依賴于一個精密而復雜的生物學過程——精子發生,其中精子變形更是決定雄性生育能力的核心環節。在這一終末分化階段,圓形的精子細胞經歷了一場劇烈的形態重塑,細胞核濃縮、頂體形成、尾部延伸等,最終轉化為具備運動與受精功能的成熟精子。
微管網絡作為細胞骨架的核心,其動態組裝、極性分布及解聚重構是驅動精子變形的關鍵。一旦微管網絡調控失常,易導致精子畸形乃至男性不育。因此,如何精準捕捉并解析這一動態過程,是生物醫學領域的重要課題之一。
免疫熒光染色技術憑借高特異性和可視化優勢,成為研究精子變形的重要手段。α-微管蛋白抗體可作為標記微管結構的精密“探針”,精準定位微管在細胞內的分布與變化。為了驗證其在精子發生研究中的應用價值,本研究選用義翹神州(Sino Biological)的高品質Alpha-Tubulin 抗體,通過嚴謹的實驗流程,深入探究了微管網絡在精子變形過程中的動態演變。
一、實驗設計與步驟
為研究微管在精子變形中的作用機制,本實驗采用了成熟的生殖細胞爬片和免疫熒光檢測技術。具體操作步驟如下:
1,樣本制備
選取健康成年雄性小鼠,實施人道處死后快速分離雙側睪丸組織。用PBS緩沖液洗去血液等雜質。然后剝離睪丸被膜。采用胰酶-膠原酶聯合消化法分離生精小管,機械吹打獲得單細胞懸液,篩選含精原細胞、初級精母細胞、次級精母細胞及圓形/長形精子細胞的混合樣本。
2,制備細胞爬片
取細胞懸液進行爬片處理,室溫靜置2h使細胞貼壁。4%多聚甲醛室溫固定30min,PBS 洗滌3次。固定后,用含0.2% Triton X-100的PBS室溫通透15min,再用PBS洗滌3次。最后加入5% BSA封閉液37℃封閉1h,阻斷非特異性結合位點。
3,免疫熒光染色
滴加α-微管蛋白抗體(購自義翹神州,貨號:101235-T38,1:200稀釋),4℃孵育過夜,確保抗體與抗原充分結合。次日復溫并PBS洗滌后,加入熒光標記的山羊抗兔二抗(1:500稀釋),37℃避光孵育1h。用DAPI染液室溫避光染核10min,PBS洗滌3次。
4,共聚焦顯微鏡觀察
抗熒光淬滅劑封片后,采用激光共聚焦顯微鏡觀察。重點捕獲精子變形的關鍵階段:圓形精子變形起始階段、頂體形成期、尾部延伸等。采集微管骨架(熒光標記)與細胞核(DAPI標記)的共定位圖像。利用ImageJ軟件分析各階段精子細胞中微管網絡的分布特征、熒光強度及聚集區域,統計微管結構異常的精子細胞比例,明確微管動態變化與精子細胞形態建成的關聯。
Note:所使用的義翹產品
產品名稱:α-微管蛋白抗體,Alpha-Tubulin Antibody, Rabbit PAb, Antigen Affinity Purified
產品貨號:101235-T38
二、實驗結果

圖1
圖1展示三通道熒光共定位結果。精子頭部的細胞核DNA標記為藍色熒光。α-微管蛋白標記為綠色,精子尾部的細胞骨架呈現出長條狀信號。紅色是線粒體膜蛋白TOMM20,顯示精子尾部出現點狀/短條狀信號。三色疊加直觀揭示了微管作為運動裝置的結構基礎。
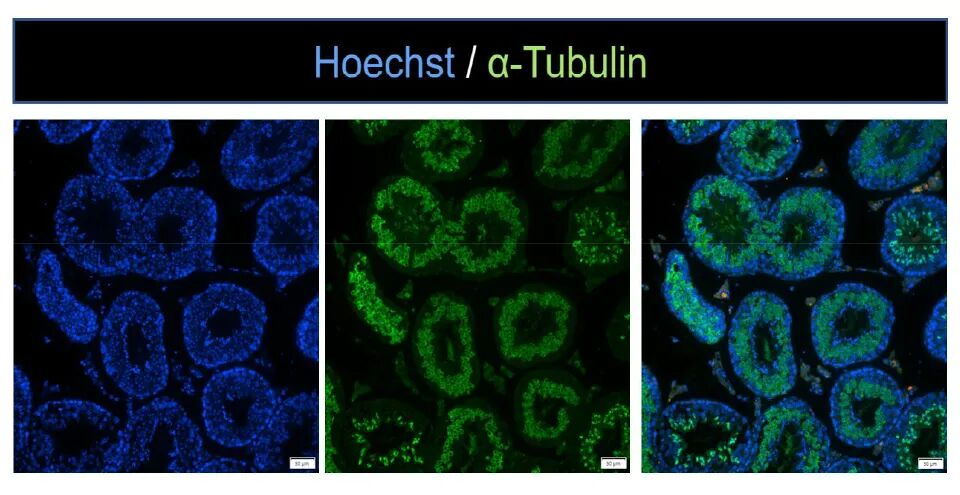
圖2
圖2為睪丸曲精小管免疫熒光染色結果。藍色(Hoechst)標記曲精小管內各級生精細胞的細胞核,清晰呈現小管的腔狀結構與細胞排布。綠色(α-Tubulin)標記微管蛋白,顯示生精細胞內的細胞骨架分布。疊加圖直觀顯示微管在生精細胞中的定位特征,反映了微管骨架在生殖細胞中的廣泛分布。

圖3
圖3進一步通過睪丸細胞涂片呈現了精子變形過程的動態演變:從圓形精子細胞到延長型精子細胞,α-微管蛋白的熒光模式由核周彌散分布逐步轉變為尾部的極化聚集,生動詮釋了微管網絡在精子變形中的時空重構特性。
三、實驗結論
在激光共聚焦顯微鏡下,我們獲得了清晰且層次分明的圖像,可以直觀地觀察到,隨著精子細胞從圓形向長形轉變,微管網絡發生了顯著的重組與延伸,真實反映了精子變形過程中的細胞骨架動態。
本研究證實,義翹神州抗α-微管蛋白抗體具有特異性和靈敏度。該抗體不僅背景信號低、信噪比高,更能精準捕捉微管在Manchette結構形成、精子尾部延伸等關鍵階段的動態分布。該抗體為深入研究精子變形過程中微管網絡的重構機制及相關調控通路提供了可靠的實驗工具,推動生殖醫學從形態觀察邁向分子機制的深入解析,為挖掘男性不育相關的潛在致病靶點提供了堅實的實驗依據與強有力的技術支撐。
實驗方案來自產品使用征文大賽用戶投稿,僅供學習交流。
免責聲明